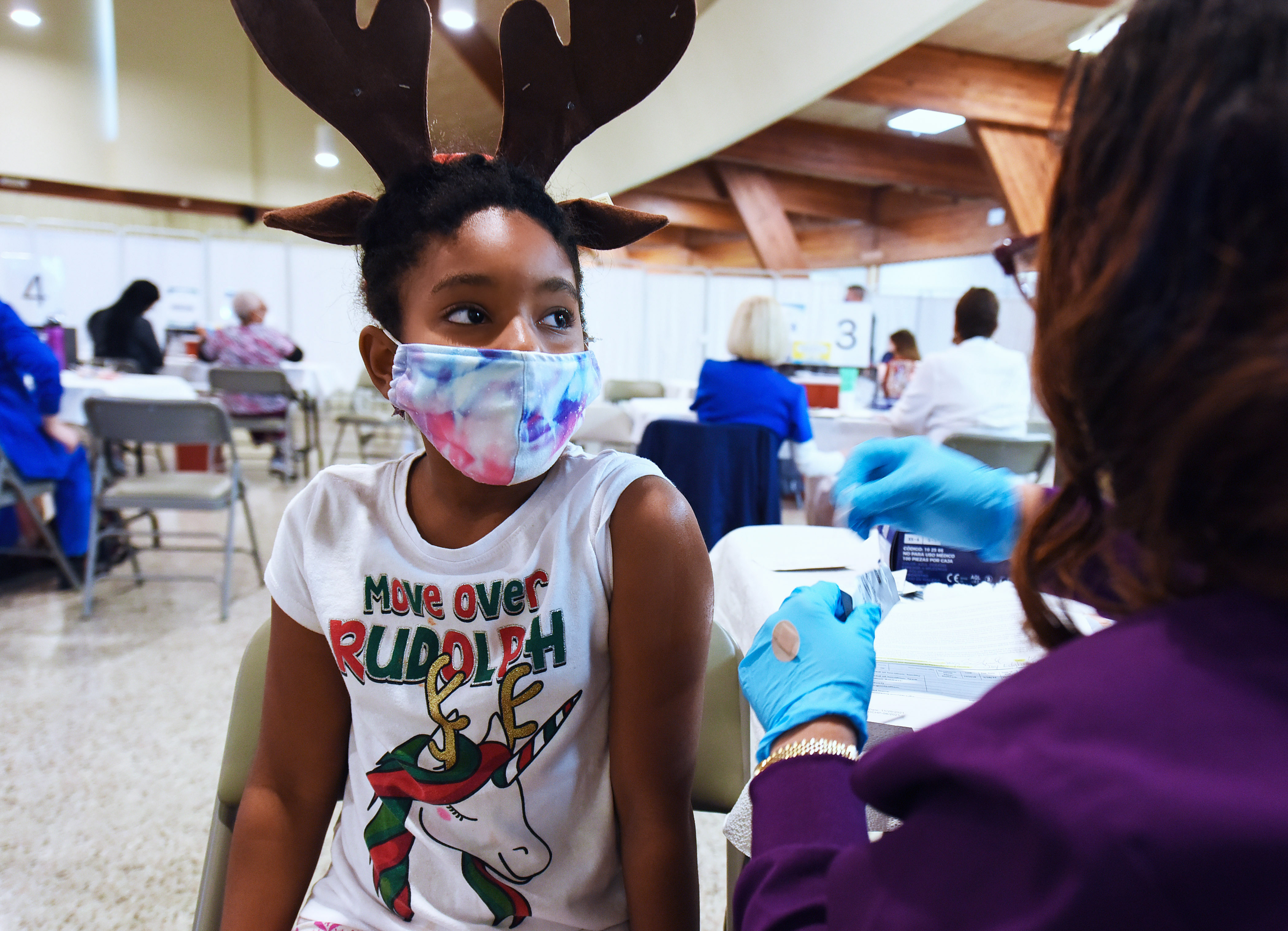
Pfizer nimmt eine dritte Dosis seines Covid-19-Impfstoffs in Studien mit dem Impfstoff bei Kindern unter 16 Jahren auf, teilte das Unternehmen am Freitag mit.
Das Unternehmen kündigte in einer Gewinnaufforderung an, eine dritte Dosis von drei Mikrogramm bei Kindern unter 5 Jahren zu testen, und in einer Pressemitteilung sagte, es plane, eine dritte Dosis von 10 Mikrogramm bei Kindern im Alter von 5 bis 11 Jahren zu testen.
Pfizer sagte, zwei Dosen des Impfstoffs führten bei Kindern im Alter von 2 bis 5 Jahren nicht zu den erwarteten Ergebnissen.
Die Impfstoffe schützten die jüngste Gruppe – Säuglinge und Kleinkinder bis zu 2 Jahren – auf dem gleichen Niveau wie bei Teenagern und jungen Erwachsenen, aber die Dosis von drei Mikrogramm erzeugte bei den 2- bis 5-Jährigen nicht dieselbe Immunität, die teilte das Unternehmen in einer Pressemitteilung mit.
„Die Entscheidung, eine dritte Dosis von 3 Mikrogramm für Kinder im Alter von 6 Monaten bis unter 5 Jahren zu evaluieren, spiegelt die Verpflichtung der Unternehmen wider, die richtige Dosis sorgfältig auszuwählen, um das Risiko-Nutzen-Profil zu maximieren“, sagte das Unternehmen.
Eine zusätzliche Studie an Jugendlichen im Alter von 12 bis 17 Jahren wird die Verwendung einer dritten Dosis von entweder 10 oder 30 Mikrogramm untersuchen, teilte das Unternehmen mit.
In den Vereinigten Staaten ist derzeit eine Auffrischimpfung des Pfizer-Impfstoffs für vollständig geimpfte Personen ab 16 Jahren erhältlich.
„Die Wirksamkeitsdaten für drei Dosen des Impfstoffs im Allgemeinen für Personen ab 16 Jahren und die frühen Labordaten, die wir mit Delta und anderen besorgniserregenden Varianten, einschließlich Omicron, gesehen haben, weisen darauf hin, dass Personen, die mit drei Dosen unseres Covid-Impfstoffs geimpft wurden, einen höheren Grad haben des Schutzes“, sagte Kathrin Jansen, Leiterin Forschung und Entwicklung bei Pfizer, in der Ausschreibung.
„Deshalb haben wir beschlossen, jede der pädiatrischen Studien um eine dritte Dosis in die Serie zu ergänzen und eine Lizenz für eine Serie mit drei Dosen anstatt wie ursprünglich erwartet für eine Serie mit zwei Dosen zu beantragen.“
Pfizer untersucht derzeit seinen Impfstoff bei Kindern im Alter von 6 Monaten bis 2 Jahren und 2 bis unter 5 Jahren. Jansen sagte, dass in einer früheren Phase von Studien für die Primärserie eine 3-Mikrogramm-Dosis in der 2- bis 5-jährigen Gruppe eine vergleichbare Immunantwort auf eine Dosis bei älteren Bevölkerungsgruppen mit weniger Nebenwirkungen als eine 10-Mikrogramm-Dosis zeigte.
Jansen sagte, die Änderung der Studien werde sich voraussichtlich nicht auf den Zeitplan für die Einführung der Notfallimpfgenehmigung in jüngeren Bevölkerungsgruppen auswirken, die noch bis Mitte 2022 angestrebt wird.
„Wenn die Drei-Dosis-Studie erfolgreich ist, erwarten Pfizer und BioNTech, den Aufsichtsbehörden Daten zur Unterstützung einer Notfallgenehmigung (EUA) für Kinder im Alter von 6 Monaten bis unter 5 Jahren in der ersten Hälfte des Jahres 2022 vorzulegen.“

Schöpfer. Hipster-freundlicher Unternehmer. Student. Freundlicher Analyst. Professioneller Schriftsteller. Zombie-Guru. Amateur-Web-Nerd.




















+ There are no comments
Add yours